SKYSCRAPER-08: tiragolumab + atezolizumab y quimioterapia para carcinoma esofágico de células escamosas
Fecha
27 ene 2026
Resumen
El estudio fase III SKYSCRAPER-08 evaluó la eficacia y seguridad de añadir la doble inmunoterapia con tiragolumab y atezolizumab a la quimioterapia de primera línea en pacientes con carcinoma esofágico de células escamosas no resecable o metastásico. Los resultados mostraron que la combinación mejoró significativamente tanto la supervivencia libre de progresión como la supervivencia global en comparación con la quimioterapia sola, con un perfil de seguridad manejable.
Autor/a

Diana Darriba
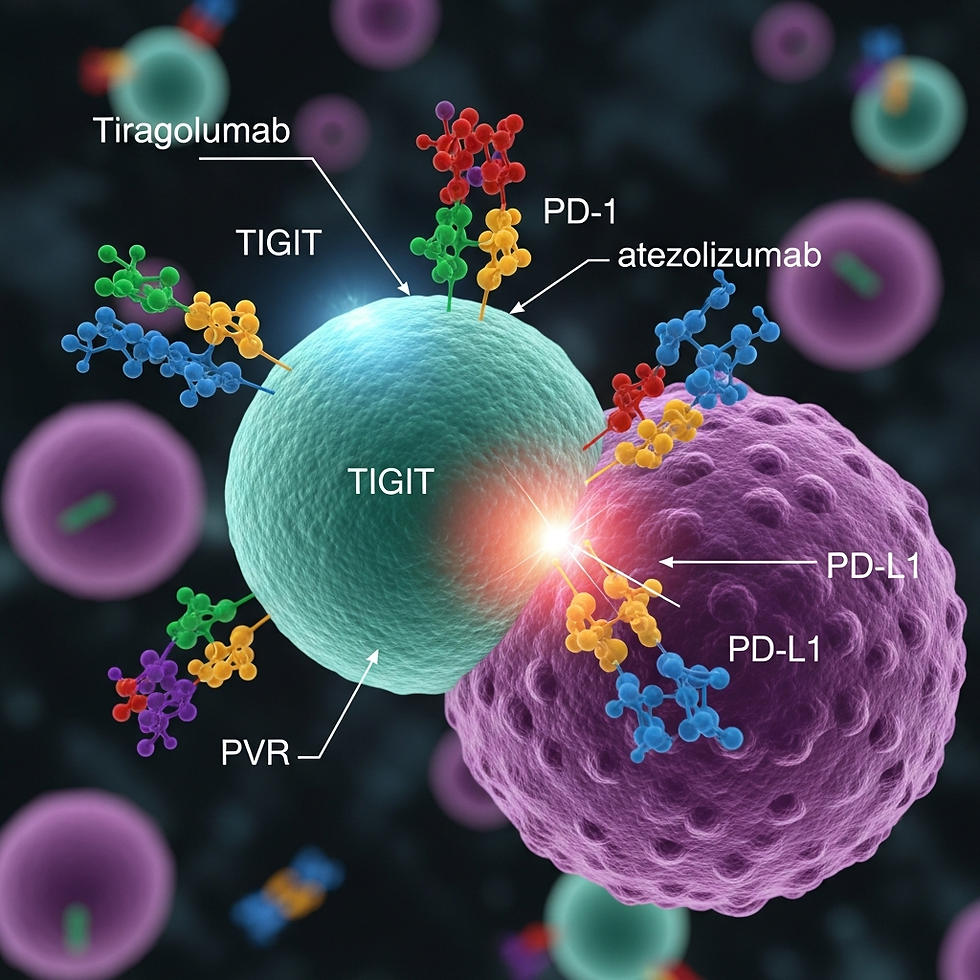
Existe una necesidad no cubierta de terapias más eficaces para pacientes con cáncer de esófago metastásico o no resecable. Una estrategia explorada es la inhibición de múltiples puntos de control inmunitario para potenciar la respuesta antitumoral. El anticuerpo monoclonal anti-TIGIT, tiragolumab, en combinación con el inhibidor de PD-L1 atezolizumab, ha mostrado resultados prometedores en tumores sólidos.
El estudio SKYSCRAPER-08 fue diseñado para evaluar si la adición de esta doble inmunoterapia a la quimioterapia estándar de primera línea confería un beneficio de supervivencia en pacientes con carcinoma esofágico de células escamosas avanzado.
🔎 ¿Qué hicieron?
El SKYSCRAPER-08 fue un ensayo fase III, internacional, aleatorizado, doble ciego y controlado con placebo, realizado en 67 centros de Asia. Se incluyeron pacientes adultos con carcinoma esofágico de células escamosas localmente avanzado no resecable, recurrente no resecable o metastásico, sin tratamiento previo.
Un total de 461 pacientes fueron aleatorizados 1:1 para recibir:
Brazo experimental (n=229): Tiragolumab (600 mg) + atezolizumab (1200 mg) + quimioterapia (paclitaxel 175 mg/m² y cisplatino 60-80 mg/m²)
Brazo control (n=232): Placebo + quimioterapia
Los objetivos primarios fueron la supervivencia libre de progresión (PFS), evaluada por un comité de revisión independiente (IRF), y la supervivencia global (OS) en la población por intención de tratar. La mediana de seguimiento de supervivencia fue de 12,6 meses.
En esta tabla resumimos la población del estudio:
Característica | Tiragolumab + Atezolizumab + QT (n=229) | Placebo + QT (n=232) |
Edad mediana (años) | 63 | 63 |
Hombres / Mujeres (%) | 87% / 13% | 89% / 11% |
ECOG 1 (%) | 75% | 74% |
Tratamiento curativo previo (%) | 36% | 36% |
Nº de órganos con metástasis ≥2 (%) | 46% | 47% |
PD-L1 ≥10% (%) | 44% | 43% |
Metástasis hepáticas (%) | 23% | 20% |
📊¿Qué encontraron?
La adición de tiragolumab y atezolizumab a la quimioterapia demostró una mejora estadísticamente significativa y clínicamente relevante en ambos objetivos primarios.

En esta tabla resumimos los resultados obtenidos:
Desenlace | Tiragolumab + Atezolizumab + QT | Placebo + QT | Hazard Ratio (HR) |
mPFS por IRF | 6,2 meses | 5,4 meses | 0,56 (IC 95%: 0,45-0,70; p<0,0001) |
mOS | 15,7 meses | 11,1 meses | 0,70 (IC 95%: 0,55-0,88; p=0,0024) |
ORR | 59,7% | 45,5% | — |
DoR | 7,1 meses | 4,3 m | — |
En los análisis de subgrupos exploratorios, el beneficio en PFS y OS se observó en la mayoría de los subgrupos preespecificados, incluyendo aquellos estratificados por expresión de PD-L1. Por ejemplo, en pacientes con PD-L1 ≥10%, la mediana de OS fue de 18,9 meses con la combinación frente a 10,5 meses con placebo (HR 0,70; IC 95%: 0,49-1,01).
⚠️¿Y en cuanto a seguridad?
El perfil de seguridad de la combinación fue consistente con los perfiles conocidos de cada fármaco individualmente. No se identificaron nuevas señales de seguridad.
Los eventos adversos (EA) de grado 3-4 ocurrieron en el 68% de los pacientes del brazo experimental frente al 61% del brazo control.
Los EA severos ocurrieron en el 41% y 39% de los pacientes, respectivamente.
Se reportaron 6 muertes relacionadas con el tratamiento (3%) en el grupo de la triple combinación (neumonitis, paro cardíaco, hemorragia gastrointestinal, fallo hepático, neumonía bacteriana y enfermedad pulmonar inmunomediada) y 2 (1%) en el grupo placebo (infección gastrointestinal y causa desconocida).
Los EA de grado 3-4 más frecuentes fueron hematológicos y similares entre ambos brazos:
EAs grado 3-4 | Tiragolumab + Atezolizumab + QT (n=228) | Placebo + QT (n=227) |
Neutropenia | 34% | 34% |
Leucopenia | 20% | 15% |
Anemia | 8% | 11% |
✅ ¿Qué concluyeron?
El estudio SKYSCRAPER-08 alcanzó sus dos objetivos primarios, demostrando que la adición de tiragolumab y atezolizumab a la quimioterapia de primera línea proporciona un beneficio de supervivencia estadísticamente significativo y clínicamente relevante en pacientes con carcinoma esofágico de células escamosas avanzado.
Estos datos respaldan la justificación de explorar la doble inhibición de puntos de control (TIGIT y PD-L1) combinada con quimioterapia como una nueva opción de tratamiento para esta población de pacientes con una alta necesidad médica no cubierta.