ASCENT-03: Sacituzumab Govitecan en cáncer de mama triple negativo sin tratamiento previo
Fecha
8 dic 2025
Resumen
El ensayo fase 3 ASCENT-03 demuestra que Sacituzumab Govitecan duplica la mediana de la DoR y prolonga significativamente la PFS frente a la quimioterapia estándar en pacientes con TNBC avanzado previamente no tratado y no apto para inhibidores de PD-1/PD-L1.
Autor/a

Diana Darriba
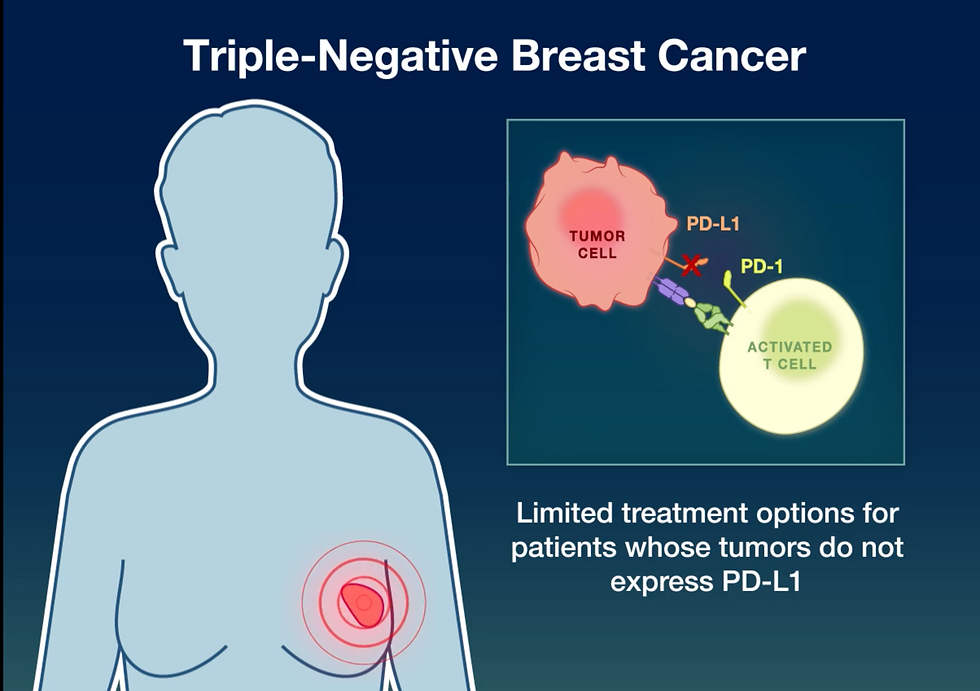
El cáncer de mama triple negativo (TNBC), caracterizado por la falta de expresión de receptores hormonales (ER/PR) y HER2, es un subtipo agresivo que representa el 10% al 15% de todos los cánceres de mama y se asocia a un pronóstico pobre.
Para las pacientes con TNBC metastásico previamente no tratado y con tumores PD-L1 negativos, las opciones son limitadas a la quimioterapia. Existe una necesidad crítica de tratamientos de primera línea más efectivos para pacientes que no son candidatas a inhibidores de PD-1/PD-L1 debido a su uso previo (en terapias adyuvantes/neoadyuvantes) o a comorbilidades preexistentes.
El antígeno de superficie de células trofoblásticas 2 (Trop-2) está altamente expresado en el TNBC y es la diana de Sacituzumab Govitecan, un conjugado anticuerpo-fármaco (ADC) que libera un potente inhibidor de la topoisomerasa I.
🧪 Diseño experimental
ASCENT-03 fue un ensayo de fase 3, internacional, abierto y aleatorizado, diseñado para comparar Sacituzumab Govitecan con quimioterapia estándar en pacientes con TNBC avanzado previamente no tratado que no eran candidatos para recibir inhibidores de PD-1/PD-L1. Participaron 558 pacientes, asignadas aleatoriamente (1:1) a uno de estos brazos:
Sacituzumab Govitecan: 10 mg/kg intravenoso en los días 1 y 8 en ciclos de 21 días.
Quimioterapia (a elección del investigador): Paclitaxel o nab-paclitaxel (taxanos) o gemcitabina más carboplatino.
El 99% de los pacientes en el brazo de Sacituzumab Govitecan y más del 99% en el de quimioterapia tenían tumores PD-L1 negativos (CPS <10).
El criterio de valoración principal fue la supervivencia libre de progresión (PFS), evaluada por revisión central independiente ciega.
📈 Resultados de eficacia
El ensayo cumplió su objetivo primario, demostrando una mejora significativa en la PFS con Sacituzumab Govitecan.
Desenlace | Sacituzumab Govitecan (N=279) | Quimioterapia (N=279) | HR estratificado (IC 95%) |
mPFS (meses) | 9,7 (8,1-11,1) | 6,9 (5,6-8,2) | 0,62 (0,50-0,77) |
ORR | 48% | 46% | - |
mDoR | 12,2 meses | 7,2 meses | - |
🔎 Análisis de subgrupos:
La PFS fue significativamente más larga con Sacituzumab Govitecan en la mayoría de los subgrupos preespecificados, incluyendo pacientes con peor pronóstico como recurrencia temprana (6-12 meses) y metástasis hepáticas.
La mediana de OS, todavía con datos inmaduros (37% de madurez), fue de 21,5 meses con Sacituzumab Govitecan y 20,2 meses con quimioterapia.
DoR diferencial: Aunque las tasas de ORR y el tiempo a la respuesta fueron similares, la duración de la respuesta fue significativamente más prolongada con Sacituzumab Govitecan (12,2 meses vs 7,2 meses).
💊 Perfil de seguridad
Evento Adverso (AE) | Sacituzumab Govitecan (N=275) | Quimioterapia (N=276) |
AE grado ≥3 | 66% | 62% |
AEs grado ≥3 más frecuentes | Neutropenia (43%), Diarrea (9%), Leucopenia (7%) | Neutropenia (41%), Anemia (16%), Leucopenia (13%) |
AE que conduce a discontinuación | 4% | 12% |
AE que conduce a reducción de dosis | 37% | 45% |
Fatalidades: Ocurrieron 7 muertes debido a AEs con Sacituzumab Govitecan; 5 casos fueron infecciones secundarias a neutropenia que ocurrieron al inicio del tratamiento (Ciclo 1 o 2) y fueron consideradas relacionadas con el tratamiento.
Neutropenia: Aunque la neutropenia fue la AE Grado ≥3 más común en ambos brazos, Sacituzumab Govitecan se asoció con menos reducciones de dosis y menos discontinuaciones que la quimioterapia.
Profilaxis: Se subraya que la neutropenia febril mortal ocurrió en pacientes con factores de riesgo (edad avanzada, comorbilidades, radioterapia previa) que no habían recibido profilaxis primaria con factor estimulante de colonias de granulocitos (G-CSF). Las guías actuales recomiendan la profilaxis primaria con G-CSF en pacientes con riesgo aumentado.
📝 Un nuevo estándar en TNBC no apto para PD-1
El ensayo ASCENT-03 establece que Sacituzumab Govitecan es una terapia de primera línea significativamente superior a la quimioterapia en pacientes con TNBC metastásico previamente no tratado y no apto para inhibidores de PD-1/PD-L1.
El beneficio es impulsado por la reducción del 38% en el riesgo de progresión o muerte y una duración de respuesta mediana duplicada. Aunque los AEs Grado ≥3 totales fueron similares a la quimioterapia, el ADC fue asociado con una tasa de discontinuación por toxicidad significativamente menor (4% vs 12%) y menos reducciones de dosis, lo que sugiere una mejor tolerabilidad.
Estos resultados, junto con el ensayo ASCENT-04, apoyan el uso de Sacituzumab Govitecan en la primera línea de tratamiento del TNBC metastásico, lo que tiene el potencial de cambiar el panorama terapéutico.
Noticias Destacadas
Podcasts
CyC
¿Estamos ante un nuevo paradigma en el cáncer de cabeza y cuello recurrente/metastásico no relacionado con VPH gracias a OrigAMI-4?