Análogos de cannabinoides con potente actividad antitumoral en cáncer de páncreas
Fecha
5 sept 2025
Resumen
Un estudio preclínico ha sintetizado y evaluado una nueva clase de análogos cannabinoides que han demostrado una potente eficacia antitumoral en modelos de laboratorio de cáncer de páncreas, además de efectos sinérgicos con el tratamiento quimioterapéutico estándar y un perfil de toxicidad favorable.
Autor/a

Diana Darriba
Un estudio preclínico ha sintetizado y evaluado una nueva clase de análogos cannabinoides que han demostrado una potente eficacia antitumoral en modelos de laboratorio de cáncer de páncreas, además de efectos sinérgicos con el tratamiento quimioterapéutico estándar y un perfil de toxicidad favorable.
El adenocarcinoma ductal de páncreas (PDAC) es una forma de cáncer agresiva y letal, con opciones de tratamiento limitadas y una baja tasa de supervivencia. El diagnóstico en etapas avanzadas, junto con la resistencia a la quimioterapia y la radioterapia, hacen que el PDAC sea un desafío clínico importante. Los tratamientos actuales, como la combinación de gemcitabina y nab-paclitaxel, solo proporcionan beneficios marginales de supervivencia y están asociados con efectos secundarios significativos.
Aunque los cannabinoides han mostrado efectos antiproliferativos en varios tipos de cáncer, su eficacia clínica en el cáncer de páncreas sigue sin explorarse. A pesar de que los compuestos naturales como el cannabidiol (CBD) y el tetrahidrocannabinol (THC) han demostrado efectos sinérgicos con la quimioterapia en modelos preclínicos, su débil actividad contra las células de cáncer de páncreas y las altas concentraciones necesarias para obtener resultados han limitado su aplicación clínica. Con este contexto, este estudio se centró en la síntesis y evaluación de nuevos análogos de cannabinoides para encontrar terapias más efectivas y menos tóxicas para el PDAC.
🥼 ¿Cómo fue la investigación?
Se sintetizaron nuevos análogos de cannabinoides, incluido el compuesto CCL-106 y sus epímeros CCL-114 y CCL-115, que tienen una estructura molecular diferente de los cannabinoides naturales conocidos como CBD y THC. Los exhaustivos estudios preclínicos incluyeron:
🧫 Ensayos de proliferación celular en modelos de cáncer de páncreas en 2D y 3D para determinar la concentración que causa el 50% de inhibición del crecimiento (IC50) y la sinergia con el régimen de quimioterapia estándar de gemcitabina y nab-paclitaxel.
👁️ Estudios mecanísticos para comprender cómo los compuestos ejercen sus efectos, centrándose en la activación de receptores y la generación de especies reactivas de oxígeno (ROS).
🔎 Estudios in vivo utilizando un modelo de xenoinjerto derivado de células (CDX) y un modelo de xenoinjerto derivado de pacientes (PDX) para evaluar la eficacia antitumoral y la toxicidad sistémica.
🔬 ¿Qué encontraron?
🛑 Potente actividad antitumoral: Los compuestos CCL-106, CCL-114 y CCL-115 demostraron valores de IC50 sustancialmente más bajos en las líneas celulares de cáncer de páncreas humano en comparación con el CBD, con una potencia de 14 a 27 veces mayor. Inhibieron significativamente la proliferación tanto en modelos celulares 2D como en 3D.
🔃 Sinergia con la quimioterapia: El CCL-106 potenció significativamente la eficacia del régimen de quimioterapia estándar de gemcitabina y nab-paclitaxel in vitro. La combinación de CCL-106 con esta quimioterapia mostró efectos sinérgicos en la inhibición del crecimiento de las células de PDAC.
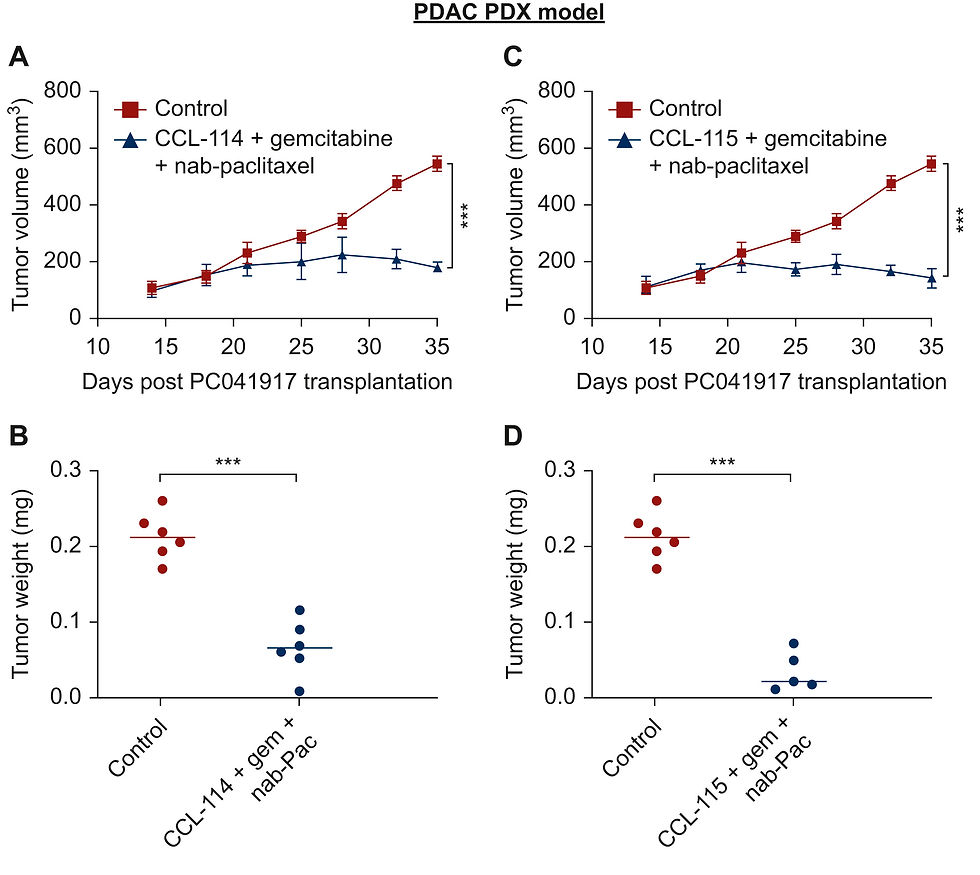
🤏 Eficacia in vivo: En un modelo PDX de cáncer de páncreas, la combinación de CCL-114 o CCL-115 con gemcitabina y nab-paclitaxel demostró una inhibición notablemente significativa del crecimiento del tumor. El CCL-106 solo redujo el volumen y el peso del tumor en aproximadamente un 51% en un modelo CDX.
▶️ Mecanismo de acción: Los efectos antiproliferativos de estos compuestos están mediados principalmente por la activación de los receptores CB2 y GPR55, además de la generación de especies reactivas de oxígeno (ROS). El receptor CB2 se asocia con respuestas antiinflamatorias y no con los efectos psicoactivos que se atribuyen al receptor CB1.
⛑️ Seguridad: El tratamiento con CCL-106 en los modelos de ratón no indujo toxicidad sistémica ni pérdida de peso sustancial en los animales.

📝 Conclusión final:
El análogo cannabinoide CCL-106 y sus epímeros, CCL-114 y CCL-115, han demostrado una potente eficacia antitumoral y efectos sinérgicos con la quimioterapia estándar en modelos preclínicos de PDAC. Su mecanismo de acción, que implica la activación de receptores CB2 y GPR55, sugiere que podrían ser opciones terapéuticas prometedoras que no inducen los efectos psicoactivos típicamente asociados con el receptor CB1.
Estos hallazgos proporcionan una base sólida para su futura investigación clínica. Se necesitan más estudios clínicos, incluido un primer ensayo de fase I en humanos, para explorar la seguridad, tolerabilidad y farmacocinética de estos compuestos en pacientes con PDAC avanzado. La capacidad de estos análogos para potenciar la quimioterapia estándar y su favorable perfil de toxicidad abren una nueva vía para desarrollar terapias más efectivas y menos tóxicas para el tratamiento de este agresivo tipo de cáncer.
Noticias Destacadas
SARCOMA
NCT04200443: Cabozantinib + temozolomida en leiomiosarcoma y otros sarcomas de tejidos blandos

HEMATOONCO
inMIND: tafasitamab + lenalidomida y rituximab en linfoma folicular en recaída o refractario
.png)